Klonierung und Expression
IMPP-Score: 0.5
Einleitung zur Klonierung und Expression rekombinanter Proteine
Die Klonierung und Expression rekombinanter Proteine sind zwei fundamentale Verfahren der molekularen Biologie und Biotechnologie. Sie ermöglichen die Herstellung von Proteinen in einem Wirtsorganismus, die sonst schwer zu gewinnen sind. Durch diese Methode können zum Beispiel Enzyme, Hormone und Antikörper hergestellt werden, die in der Medizin und Forschung von großer Bedeutung sind.
DNA-Klonierung: Einsatz von Plasmiden, Bakteriophagen und Liposomen
Bei der DNA-Klonierung wird genetisches Material (DNA) in einen Vektor eingeführt, der in einen Wirtsorganismus eingeschleust wird, um dort das gewünschte Protein zu produzieren.
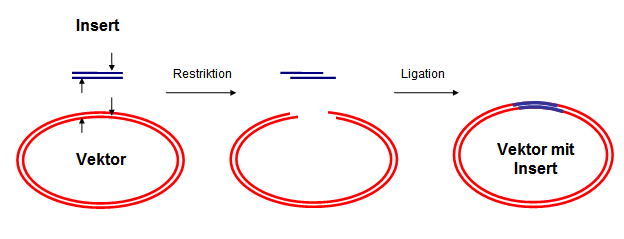
Es gibt verschiedene Typen von Vektoren, die dafür genutzt werden können:
Plasmide sind kleine, ringförmige DNA-Moleküle, die unabhängig von der chromosomalen DNA in Bakterien vorhanden sind. Durch die Transformation, also die Aufnahme von Plasmid-DNA durch die Bakterienzelle, kann Fremd-DNA in die Zelle eingebracht und exprimiert werden.
Bakteriophagen sind Viren, die Bakterien infizieren. Man kann sie nutzen, um Fremd-DNA in Bakterien einzuschleusen, indem die virulenten Eigenschaften des Phagen deaktiviert werden und stattdessen Fremd-DNA in das Bakterium eingebracht wird.
Liposomen sind künstlich hergestellte Lipidvesikel, die genutzt werden können, um DNA durch die Zellmembran von Eukaryoten (beispielsweise in tierischen Zellen) einzubringen. Dies geschieht oft durch Endozytose.
Klonierungsvektoren: Eigenschaften und Auswahl
Klonierungsvektoren sind entscheidend für den Erfolg der Klonierung. Sie müssen sicherstellen, dass die Fremd-DNA stabil in den Wirtsorganismus eingebracht wird und effizient exprimiert werden kann.
Auswahlkriterien hierfür sind unter anderem die Größe des einzubringenden DNA-Fragments, die Kompatibilität mit dem Wirtsorganismus und die Fähigkeit des Vektors, die Expression des Proteins zu steuern.
Die Ligasen spielen eine wichtige Rolle beim Klonieren, weil sie DNA-Fragmente, die durch Restriktionsenzyme erzeugt wurden, wieder verbinden können. Diese Enzyme katalysieren die Bildung von Esterbindungen zwischen den Zucker- und Phosphatgruppen der DNA, was eine stabile Integration in den Vektor ermöglicht.
Expressionssysteme für rekombinante Proteine
Die Wahl des richtigen Expressionssystems ist entscheidend für die effiziente Produktion des rekombinanten Proteins.
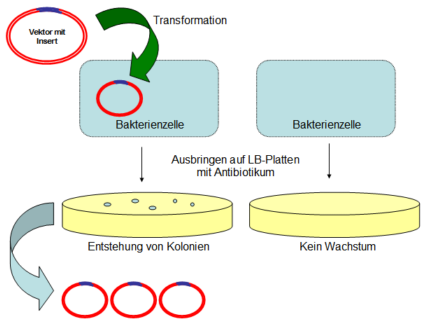
Hier sind einige der gängigen Systeme:
E. coli ist ein weit verbreitetes System aufgrund seiner einfachen Handhabung und schnellen Wachstumsrate. Allerdings kann E. coli keine komplexen posttranslationalen Modifikationen durchführen.
CHO-Zellen (chinese hamster ovary cells) werden häufig in der pharmazeutischen Industrie verwendet, da sie fähig sind, fast alle Arten von posttranslationalen Modifikationen durchzuführen und somit sehr menschenähnliche Proteine produzieren können.
Hefen, wie Saccharomyces cerevisiae, bieten eine gute Balance, da sie einfacher als Säugetierzellen zu handhaben sind und einige posttranslationale Modifikationen durchführen können.
Pflanzliche Systeme und Insektenzellen werden auch genutzt, vor allem wenn spezifische Vorteile wie Kosten und Sicherheit eine Rolle spielen oder spezielle posttranslationale Modifikationen erforderlich sind.
Praxisbezug und realweltliche Anwendungen
Rekombinante Proteintechnologie hat revolutionäre Anwendungen in der Medizin und Industrie ermöglicht. Beispiele hierfür sind:
Die Herstellung von Insulin, Impfstoffen und monoklonalen Antikörpern, die in der Behandlung von Krankheiten wie Diabetes und Krebs eingesetzt werden.
Die Produktion von Enzymen, die in Waschmitteln verwendet werden oder um biologische Prozesse in der Lebensmitteltechnologie zu verbessern.
Das IMPP fragt besonders gern nach den Unterschieden zwischen den Expressionssystemen und ihren spezifischen Vor- und Nachteilen für die Proteinexpression. Hier ist es besonders wichtig, dass ihr die Fähigkeiten zur posttranslationalen Modifikation in den verschiedenen Systemen versteht.
Dieser umfassende Überblick soll euch helfen, die Konzepte der Klonierung und Expression besser zu verstehen und für eure Prüfungen und zukünftige Forschungsprojekte optimal vorbereitet zu sein.
Zusammenfassung
Feedback
Melde uns Fehler und Verbesserungsvorschläge zur aktuellen Seite über dieses Formular. Vielen Dank ❤️
Footnotes
Credits Schematische Darstellung einer Klonierung mit Restriktion und Ligation. Grafik: The original uploader was Andymuc at German Wikipedia., Klonierung2, CC BY-SA 3.0↩︎
Credits Schematische Darstellung der Transformation einer rekombinanten DNA in eine Bakterienzelle und anschließender Antibiotika-Selektion. Grafik: The original uploader was Andymuc at German Wikipedia., Transformation2, CC BY-SA 3.0↩︎
