Flüssigchromatographie Grundlagen
IMPP-Score: 3.5
Grundlagen der Flüssigchromatographie und Säulencharakteristika
Die Flüssigchromatographie, speziell die Hochleistungsflüssigchromatographie (HPLC), ist eine leistungsfähige Methode zur Trennung und Analyse von Mischungen chemischer Substanzen. Sie basiert auf den Wechselwirkungen der Moleküle in der Probe mit einer stationären Phase und einer mobilen Phase. Die Säulencharakteristika, wie die Art der stationären Phase und die Partikelgröße, spielen dabei eine zentrale Rolle.
Das Konzept der Retentionszeit
Die Retentionszeit (\(t_R\)) ist die Zeitspanne, die eine Substanz benötigt, um durch die Säule zu wandern. Sie wird beeinflusst durch die Wechselwirkungen der Substanz mit der stationären Phase und der mobilen Phase. Starke Wechselwirkungen mit der stationären Phase führen zu längeren Retentionszeiten. Der Retentionsfaktor (\(k\)) kann aus der Formel \(k = (t_R - t_0) / t_0\) berechnet werden, wobei \(t_0\) die Totzeit ist.
Verschiedene stationäre Phasen und ihre Anwendungsbereiche
- Kieselgel und Aluminiumoxid: Häufig verwendete Materialien für die stationäre Phase in der Normalphasenchromatographie, bei der polare Phasen eingesetzt werden.
- RP-Kieselgel (Reverse Phase): Durch Oberflächenderivatisierung hydrophob gemachtes Kieselgel, z.B. mit Silanen wie Chlorsilanen. Diese Art der stationären Phase wird hauptsächlich in der Umkehrphasenchromatographie (RPC) eingesetzt. Unpolare Verbindungen werden bevorzugt von der stationären Phase zurückgehalten, während polare Moleküle schneller eluieren.
- Cyanopropyl-Phase: Eine weitere Variante des modifizierten Kieselgels, das für spezifische Trennungen nach Polarität oder speziellen Wechselwirkungen genutzt wird.
Um aus Kieselgel ein Umkehrphasenmaterial für die RP-HPLC zu erhalten, müssen dessen Silanolfunktionen effektiv hydrophobisiert werden. Dies geschieht durch Oberflächenderivatisierung, oft mit Chlorsilanen, da sie eine hohe Reaktivität aufweisen und das Chloridion eine gute Abgangsgruppe darstellt.
Einfluss der Partikelgröße
Die Partikelgröße der stationären Phase hat direkte Auswirkungen auf die Trenneffizienz und den Säulendruck: - Kleinere Partikelgrößen erhöhen die Oberfläche, was zu einer höheren Trenneffizienz führt, aber auch den Säulendruck erhöht. - Die Bodenzahl (\(N\)) einer Säule, ein Maß für die Trenneffizienz, errechnet sich aus \(N = 5,54 * (t_R / w_{h})^2\), wobei \(w_{h}\) die Peakbreite in halber Höhe ist.
Chromatographische Verfahren
- Normalphasenchromatographie: Verwendung einer polaren stationären Phase und einer weniger polaren mobilen Phase. Polare Substanzen werden stärker zurückgehalten.
- Umkehrphasenchromatographie (RPC): Einsatz einer unpolaren (hydrophoben) stationären Phase und einer polaren mobilen Phase. Hier werden unpolare Moleküle stärker zurückgehalten.
- Ionenchromatographie: Spezialisiert auf die Trennung von Ionen durch den Einsatz von Ionenaustauscherharzen.
- Größenausschlusschromatographie: Trennt Moleküle auf Basis ihrer Größe durch Einsatz von Porensieben.
Zur Trennung von Enantiomeren werden oft spezialisierte stationäre Phasen eingesetzt, die auf chiralen Wechselwirkungen basieren. Dies ermöglicht die Trennung von Molekülen, die sich nur in ihrer räumlichen Anordnung unterscheiden.
Das IMPP fragt gerne nach den spezifischen Wechselwirkungen zwischen Analyt und stationärer Phase und der Bedeutung der Partikelgröße für den Trennprozess. Ein solides Verständnis der unterschiedlichen chromatographischen Verfahren und ihrer Anwendungen, besonders in der Analyse von Enantiomeren, ist hier von Vorteil.
Betriebsmodi und Detektionsmethoden in der Flüssigchromatographie
Isokratische und Gradientenelution
Die Hochdruckflüssigchromatographie (HPLC) ist eine zentrale Methode zur Trennung von Molekülen in der analytischen Chemie. Eine wesentliche Unterscheidung liegt in den Betriebsmodi: der isokratischen und der Gradientenelution.
Bei der isokratischen Elution bleibt die Zusammensetzung der mobilen Phase während des gesamten Analysevorgangs unverändert. Dieser Modus eignet sich besonders für die Trennung von Proben mit ähnlichen Retentionszeiten und ist aufgrund seiner Einfachheit und Vorhersagbarkeit beliebt. Ein klassisches Beispiel hierfür ist die Trennung von Molekülen, die sich in der Polarität nur geringfügig unterscheiden, auf einer Normalphase.
Im Gegensatz dazu wird bei der Gradientenelution die Zusammensetzung der mobilen Phase im Lauf der Zeit verändert, typischerweise von einem polaren zu einem weniger polaren Lösungsmittel. Diese Methode verbessert die Trennleistung und ist besonders effektiv bei der Trennung komplexer Proben mit einer breiten Palette von Polaritäten. Die Gradientenelution wird häufig in der Umkehrphasenchromatographie (RPC) angewendet, wo die stationäre Phase unpolar ist und die mobilen Phasen mit der Zeit an Polarität verlieren, um Retentionszeiten zu reduzieren und Peaks zu schärfen.
Die Auswahl zwischen isokratischer und Gradientenelution hängt stark von der Probe und dem Ziel der Analyse ab. Für komplexere Mischungen wird oft eine Gradientenelution bevorzugt, um eine höhere Trennleistung zu erzielen.
Detektionsmethoden
In der Flüssigchromatographie kommt der Detektion der getrennten Komponenten eine Schlüsselrolle zu. Verschiedene Detektionsmethoden finden Anwendung, abhängig von den Eigenschaften der zu analysierenden Moleküle.
UV-Vis-Detektion
Die UV-Vis-Spektroskopie ist eine der häufigsten Detektionsmethoden in der HPLC. Sie basiert auf dem Absorptionsverhalten von Molekülen im ultravioletten (UV) und sichtbaren (Vis) Spektralbereich. Viele organische Moleküle zeigen bei spezifischen Wellenlängen signifikante Absorptionen, die zur Detektion genutzt werden können. Diese Methode ist besonders effektiv für Substanzen mit Chromophoren. Probleme treten jedoch auf, wenn Moleküle bei der gewählten Detektionswellenlänge nicht absorbieren.
Fluorimetrie
Die Fluorimetrie wird für Analyten angewendet, die fluoreszieren können. Nach der Anregung durch Licht einer bestimmten Wellenlänge emittieren diese Moleküle Licht einer längeren Wellenlänge. Diese Methode zeichnet sich durch ihre hohe Empfindlichkeit und Selektivität aus.
Amperometrie
Die Amperometrie ist eine elektrochemische Detektionsmethode, die Nutzen aus der Oxidierbarkeit oder Reduzierbarkeit von Analyten zieht. Sie ist besonders relevant für Moleküle, die durch UV-Vis-Detektion oder Fluorimetrie nicht leicht nachweisbar sind.
Die UV-Vis-Detektion wird häufig verwendet, kann jedoch durch Direkt- und Derivatisierungsmethoden ergänzt werden, um auch die Detektion von Substanzen zu ermöglichen, die bei bestimmten Wellenlängen nicht detektierbar sind.
UV-Cut-off-Wert
Der UV-Cut-off-Wert eines Lösungsmittels ist die Wellenlänge, unter der das Lösungsmittel beginnt, UV-Licht wesentlich zu absorbieren. Die Wahl des Lösungsmittels für die mobile Phase unter Berücksichtigung seines UV-Cut-off-Wertes ist entscheidend, um Interferenzen mit der Detektion zu vermeiden. Lösungsmittel mit niedrigem UV-Cut-off sind bevorzugt, wenn Analyte bei niedrigen Wellenlängen detektiert werden sollen.
Temperatur- und Polaritätseffekte sowie Peakqualität und -analyse
Temperaturabhängigkeit in der HPLC
Die Hochleistungsflüssigchromatographie (HPLC) ist stark temperaturabhängig. Eine Erhöhung der Temperatur kann beispielsweise die Viskosität der mobilen Phase verringern. Dies führt dazu, dass die mobile Phase leichter durch die Säule fließt, was wiederum die Retentionszeiten der Analyte verkürzt. Eine niedrigere Viskosität bedeutet auch einen niedrigeren Druck in der Säule und in einigen Fällen verbesserte Trennleistungen durch schärfere und höhere Peaks.
Polaritätseffekte
In der HPLC spielt die Polarität der mobilen Phase, der stationären Phase und der Analyte eine wichtige Rolle. Bei der Umkehrphasenchromatographie (Reverse Phase, RP) zum Beispiel sind die stationären Phasen im Allgemeinen unpolare (hydrophobe) Oberflächen, wohingegen die mobile Phase wasserbasiert ist. Die Retention der Analyte wird durch ihre Wechselwirkung mit der stationären und mobilen Phase bestimmt. Substanzen mit einer höheren Affinität zur stationären Phase werden länger zurückgehalten als solche, die eine stärkere Wechselwirkung mit der mobilen Phase aufweisen.
Die Polarität der mobilen Phase kann durch das Hinzufügen organischer Lösungsmittel wie Acetonitril oder Methanol modifiziert werden, um die Elutionskraft zu erhöhen oder zu reduzieren.
Peakqualität: Tailing und Symmetrie
Ein Problem, das oft in der HPLC auftritt, ist das sogenannte Peak-Tailing. Dieses Phänomen, bei dem die abfallende Flanke eines Peaks verzögert erscheint, kann durch unterschiedliche Faktoren verursacht werden, einschließlich Interaktionen mit der stationären Phase oder Totvolumen im System. Eine symmetrische Peakform ist ideal, da sie eine präzise Quantifizierung ermöglicht. Die Form der Peaks kann durch Änderungen der Temperatur, der Fließgeschwindigkeit oder der Zusammensetzung der mobilen Phase angepasst werden.
Schlüsselparameter für die Peak-Analyse
- Auflösung (RS): Maß für die Trennung zweier benachbarter Peaks. Eine höhere Auflösung bedeutet, dass zwei Peaks besser voneinander getrennt sind.
- Retentionsfaktor (k): Verhältnis der Zeit, die ein Analyt in der stationären Phase verbringt, zur Zeit, die er in der mobilen Phase verbringt. Ein höherer k-Wert bedeutet eine stärkere Retention.
- Totzeit (t0): Zeit, die für ein nicht-retardiertes Molekül benötigt wird, um die Säule zu passieren.
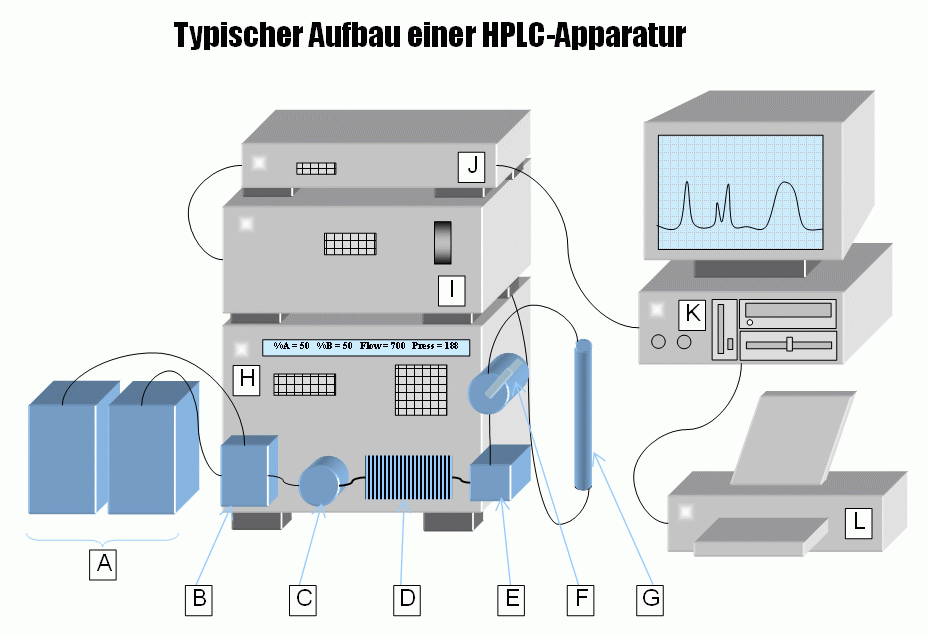
Geräteauffbau und Vorsäulen
Ein korrekter Geräteauffbau ist entscheidend, um optimale Ergebnisse in der HPLC zu erzielen. Die Verwendung von Vorsäulen kann helfen, die Lebensdauer der analytischen Säule zu verlängern, indem sie Partikel und hochmolekulare Verbindungen abfängt, die sonst die stationäre Phase beschädigen könnten.
Zusammenfassung
Feedback
Melde uns Fehler und Verbesserungsvorschläge zur aktuellen Seite über dieses Formular. Vielen Dank ❤️
Footnotes
Credits Aufbau einer HPLC. Grafik: ConHelius, HPLC, CC BY-SA 2.5↩︎