Elektrophoretische Verfahren
IMPP-Score: 2.3
Die Kapillarelektrophorese (CE)
Die Kapillarelektrophorese (CE) ist ein hochentwickeltes analytisches Trennverfahren, das auf der elektrophoretischen Mobilität geladener Teilchen in einem elektrischen Feld beruht. Bei diesem Prozess spielen physikalisch-chemische Eigenschaften wie Größe, Ladung und Form der Moleküle eine wesentliche Rolle. Aber wie genau hängen diese Eigenschaften mit der CE zusammen? Und warum ist das so relevant für die Trennung von Analytmolekülen?
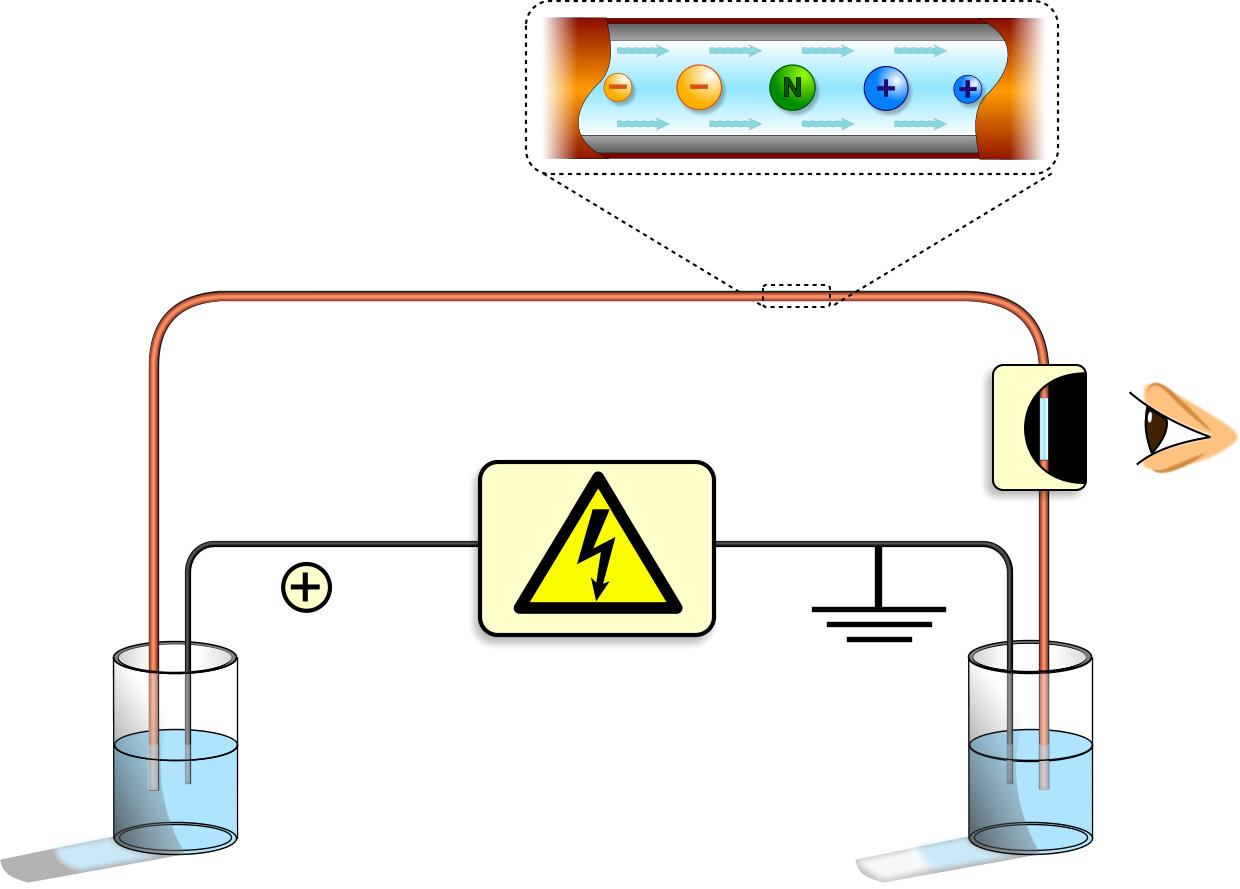
Physikalische Grundlagen der Kapillarelektrophorese
Die elektrophoretische Mobilität ist das Schlüsselelement der CE und beschreibt, wie schnell und in welche Richtung sich geladene Teilchen unter Einfluss eines elektrischen Feldes bewegen. Diese Mobilität hängt stark von der Ladung der Teilchen und ihrer Größe ab - je größer die Ladung und je kleiner das Teilchen, desto schneller bewegt es sich durch eine Kapillare. Aber auch die Form der Moleküle, der verwendete Puffer und selbst die Beschichtung der Kapillare beeinflussen die Mobilität.
Bei der Vorbereitung der Kapillarelektrophorese ist die Auswahl des Puffers und der Kapillarbeschichtung entscheidend, um optimale Mobilitäts- und damit Trennbedingungen für deine Analyte zu schaffen.
Der Elektroosmotische Fluss (EOF)
Ein zentraler Begriff in der CE ist der Elektroosmotische Fluss (EOF). Der EOF ist eine Bewegung des Lösungsmittels entlang der Kapillare, die durch Ladungen an der Kapillaroberfläche verursacht wird und somit zur Trennung beiträgt. Zur Bestimmung und Kontrolle des EOF können markierende Substanzen eingesetzt werden, die ungeladen sind und deren Bewegung ausschließlich vom EOF beeinflusst wird. Die Kontrolle des EOF ist für die Optimierung der Trennleistung unerlässlich.
Der EOF kann die Trenneffizienz der Kapillarelektrophorese bedeutend verbessern, indem er zur gleichmäßigen Verteilung der Analyte in der Kapillare beiträgt.
Spezielle Anwendungen der Kapillarelektrophorese
Dank ihrer Flexibilität findet die CE Anwendung in einer Vielzahl von Bereichen. So ermöglicht die CE beispielsweise die Trennung racemischer Gemische durch den Einsatz chiraler Selektoren. Darüber hinaus spielt der pH-Wert eine wesentliche Rolle bei der CE, da er die Ladung und damit die Wanderungsgeschwindigkeit und -richtung der Moleküle beeinflussen kann. Selbst komplexere molekulare Wechselwirkungen, wie die Bindung von Proteinen an Liganden, können mit der CE analysiert werden.
Einsatzgebiete der CE, wie in der Pharmazie, Biotechnologie und Umweltanalytik, unterstreichen die Vielseitigkeit dieses Verfahrens. Die Wahl der Kapillarbeschichtung, beispielsweise zur Reduzierung von Proteinadsorption, und der Einsatz von markierenden Substanzen zur EOF-Bestimmung sind nur einige Beispiele, wie die CE an spezifische analytische Herausforderungen angepasst werden kann.
Die Anpassung des pH-Werts im Puffer ist entscheidend für die effektive Trennung von Molekülen mit unterschiedlichen Ladungen. Eine genaue Einstellung kann die Wanderungsrichtung und -geschwindigkeit signifikant beeinflussen.
Zusammenfassung
Die Kapillarelektrophorese ist ein vielseitiges und sensibles Trennverfahren, das auf elektrophoretischer Mobilität basiert. Die Feinabstimmung physikalisch-chemischer Variablen wie dem Puffer, der Kapillarbeschichtung und dem EOF erlaubt eine hochpräzise Analyse und Trennung von Molekülen. Dies macht die CE zu einem unverzichtbaren Werkzeug in vielen wissenschaftlichen und industriellen Laboratorien.
Mizellare Elektrokinetische Chromatographie (MEKC): Theorie und Anwendung
Grundprinzipien der MEKC
Die mizellare elektrokinetische Chromatographie (MEKC) ist eine leistungsfähige Methode der Kapillarelektrophorese, die die Trennung und Analyse von chemischen Verbindungen, darunter geladene sowie ungeladene Teilchen, basierend auf ihren Wechselwirkungen mit Mizellen ermöglicht. Im Kern der MEKC steht die Verwendung von Tensiden, die bei Erreichung einer bestimmten Konzentration, der kritischen Mizellbildungskonzentration (CMC), Mizellen bilden. Ein häufig eingesetztes Tensid zur Mizellenbildung ist Natriumdodecylsulfat (SDS).
Die Rolle von Mizellen in der MEKC
Die gebildeten Mizellen agieren als eine pseudostationäre Phase. Sie bieten eine hydrophobe Umgebung an, welche die Aufnahme und Trennung hydrophober Substanzen aus der umgebenden wässrigen Phase ermöglicht. Umgangssprachlich kann man sich Mizellen als “Mini-Waschmaschinen” vorstellen, die hydrophobe Moleküle “einfangen” und durch die Kapillare transportieren. Somit spielt nicht nur die Ladung der Analyten, sondern auch ihre Hydrophobie eine Rolle bei der Trennung durch MEKC.
Unterscheidung von Analyten
Geladene und ungeladene Analyte interagieren unterschiedlich mit den Mizellen, was auf ihre unterschiedlichen Verteilungskoeffizienten zurückzuführen ist. Geladene Teilchen können durch elektrostatische Wechselwirkungen mit den Mizellen assoziieren, während ungeladene Teilchen vorwiegend aufgrund ihrer hydrophoben Eigenschaften Aufnahme in die Mizellen finden. Die MEKC erlaubt es uns daher, eine mittels traditioneller Kapillarelektrophorese schwer zu erreichende Trennung hydrophober Verbindungen zu realisieren.
Beeinflussende Faktoren der Effizienz und Auflösung
Die Trenneffizienz und Auflösung in der MEKC werden durch verschiedene Faktoren beeinflusst, darunter: - Konzentration des Tensids - Art des Tensids (z.B. SDS) - Wahl des Puffersystems - Pufferkonzentration
Direkt beeinflusst wird die Effizienz durch die Konzentration des Tensids. So sollte die Tensidkonzentration über der CMC liegen, um eine stabile Mizellbildung zu gewährleisten. Weiterhin spielt der Puffer eine Schlüsselrolle, da dieser die Bedingungen wie pH-Wert und Ionenstärke vorgibt, welche die Ladungsverhältnisse und somit die Wechselwirkungen der Analyte mit den Mizellen beeinflussen können.
Anwendungsbereiche der MEKC
Die MEKC findet breite Anwendung in der Analytik, unter anderem bei der Trennung und Analyse von: - Arzneimitteln - Pestiziden - Natürlichen Produkten
Der Vorteil der MEKC liegt vor allem in der Möglichkeit, komplexe Mischungen in einem einzigen Lauf zu trennen. Dies ermöglicht insbesondere in der Pharmazie und der Umweltanalytik eine effiziente und schnelle Analyse von Wirkstoffen und Kontaminanten.
MEKC gegenüber traditionellen Methoden
Die MEKC stellt gegenüber traditionellen chromatographischen Methoden wie der Hochdruckflüssigchromatographie (HPLC) eine kostengünstigere und zeitsparendere Alternative dar, insbesondere wenn es um die Trennung einer Vielzahl von Substanzen geht, einschließlich solcher, die keine ausgeprägte Ladung besitzen. Ihr Potenzial, sowohl geladene als auch ungeladene Analyte zu trennen, macht die MEKC zu einer wertvollen Ergänzung im Arsenal analytischer Trenntechniken.
Zusammenfassung
Feedback
Melde uns Fehler und Verbesserungsvorschläge zur aktuellen Seite über dieses Formular. Vielen Dank ❤️
Footnotes
Credits Prinzip der Kapillarelektrophorese Grafik: Andreas Dahlin, Capillary electrophoresis (21589986780), CC BY 2.0↩︎
