Cyclische Verbindungen
IMPP-Score: 1.9
Die Stereochemie cyclischer Verbindungen und deren Konformationsisomerie
Grundlagen der Konformationen
Bei der Betrachtung cyclischer Verbindungen kommt der Stereochemie eine besondere Bedeutung zu, da die räumliche Anordnung der Atome die physikalischen und chemischen Eigenschaften stark beeinflussen kann. Bevor wir uns die Details anschauen, ist es wichtig, die Grundlagen zu verstehen.
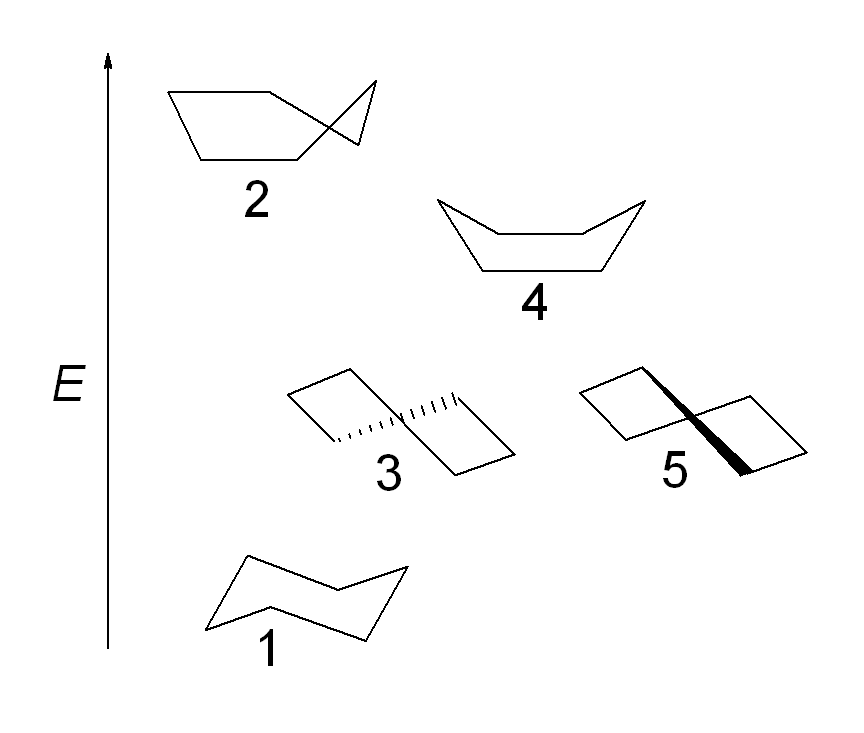
Cyclische Verbindungen, insbesondere Cyclohexane, haben aufgrund ihrer sechsgliedrigen Ringstruktur ein besonderes Verhalten in Bezug auf Konformationen. Stell dir das Cyclohexanmolekül wie einen dreidimensionalen Körper vor, der unterschiedliche Formen annehmen kann. Die flexibelsten und bedeutendsten Konformationen sind die Sessel-, Wannen- und Twistkonformationen.
Die Sesselkonformation von Cyclohexanen

Die Sesselkonformation von Cyclohexan ist besonders stabil, weil sie die sterischen Spannungen minimiert und nahezu ideale Tetraederwinkel aufweist.
Stell dir die Sesselkonformation wie einen bequemen Liegestuhl vor – die Atome sind so angeordnet, dass sie sich maximal entspannen können. Diese Form hat die niedrigste Energie, weil alle Wasserstoffatome gestaffelt zueinanderstehen und somit die van-der-Waals-Abstoßungen am kleinsten sind.
Axiale und äquatoriale Positionen von Substituenten
Bei Cyclohexanen unterscheiden wir zwischen axialen und äquatorialen Positionen der Substituenten. Axial bezeichnet Positionen, die entlang der vertikalen Achse orientiert sind – sie stehen quasi senkrecht auf der Ringebene. Äquatorial bedeutet hingegen, dass die Substituenten sich sozusagen in der Ebene des Rings befinden, sie sind also mehr seitlich ausgerichtet.
Äquatoriale Positionen sind energetisch günstiger als axiale, da sie weniger sterische Wechselwirkungen verursachen – besonders bei großen Substituenten wie tertiären Butylgruppen.
1,3-diaxiale Wechselwirkungen
Ein zentrales Phänomen der Stereochemie bei Cyclohexanen sind die 1,3-diaxialen Wechselwirkungen. Sie wird auch Prelog-Spannung genannt. Sie treten auf, wenn Substituenten an axialen Positionen nahe beieinanderstehen und sind ein Hauptgrund dafür, dass die axiale Anordnung oft energetisch ungünstig ist. Stell dir vor, zwei Menschen stehen sich in einem engen Abteil gegenüber – es ist unbehaglich und es gibt wenig Raum. Das ist vergleichbar mit axialen Substituenten, die sich “in die Quere” kommen.
Konformationsgleichgewichte
Eines der spannendsten Themen in der Stereochemie ist das Konformationsgleichgewicht. Bei Cyclohexanen bedeutet das, dass sich die Moleküle ständig zwischen verschiedenen Konformationsisomeren umwandeln, meist zwischen verschiedenen Sesselkonformationen. Dabei fluktuiert die Position von Substituenten zwischen axial und äquatorial.
Ringspannung und ihre Konsequenzen
Die Größe des Ringes und die Anordnung der Atome bestimmen die Ringspannung. Abweichungen von idealen Bindungswinkeln führen in kleinen Ringen wie Cyclopropanen und Cyclobutanen zu hoher Spannung und beeinflussen die Stabilität der Verbindungen.
Cyclohexan in der Sesselkonformation zeigt hingegen, wie gut ein sechsgliedriger Ring ideale Bindungswinkel und geringe Torsionsspannungen erreichen kann.
Chiralität bei cyclischen Verbindungen
Bei asymmetrischer Substituentenanordnung kann es auch zu Chiralität kommen. Eine Verbindung ist chiral, wenn sie nicht mit ihrem Spiegelbild zur Deckung gebracht werden kann. Im Ringkontext ergibt sich Chiralität, wenn asymmetrische Atome vorhanden sind oder die räumliche Anordnung der Substituenten keine Spiegelebene zulässt.
Bei Spirocyklen und bestimmten anderen Ringstrukturen kann axiale Chiralität auftreten, die durch asymmetrische Anordnungen von Atomen oder Substituenten entlang einer Achse definiert
Konfiguration und Konformation
Das Verständnis dieser beiden Begriffe ist entscheidend für das Erkennen von Stereoisomeren. Während man sich Konventionen durch Drehungen um einzelne Bindungen vorstellen kann, bezieht sich die Konfiguration auf die permanente Anordnung von Atomen, die nur durch das Brechen und Neubilden von Bindungen verändert werden kann. Bei disubstituierten Cyclohexanen wird zum Beispiel zwischen cis- (beide Substituenten auf der gleichen Seite der Ringebene) und trans-Konfigurationen (Substituenten auf gegenüberliegenden Seiten) unterschieden.
Bedeutung für Reaktionen
Die räumliche Anordnung in cyclischen Verbindungen beeinflusst auch ihr Reaktionsverhalten. So kann eine cis-trans-Konfiguration bestimmen, ob eine Eliminierungsreaktion zur Bildung einer Doppelbindung führt. Auch die Reaktion mit OsO4, das sich bevorzugt an cis-Doppelbindungen addiert, um cis-Diole zu bilden, ist ein praktisches Beispiel.
Das IMPP fragt besonders gerne nach den Details der Sesselkonformation, der Unterscheidung zwischen axialen und äquatorialen Positionen sowie der Auswirkung von Substituenten auf die Ringstabilität.
Bredt’sche Regel
Die Bredt’sche Regel beschreibt eine Besonderheit bei der Ausbildung von Doppelbindungen in gespannten bicyclischen Systemen. Sie besagt, dass an Brückenkopfatomen keine Doppelbindungen vorkommen, da die Spannung zu groß wäre. Dies solltet ihr insbesondere bei der Untersuchung von sterisch anspruchsvollen Strukturen wie Bicycloalkenen im Kopf behalten.
Zusammenfassung
Feedback
Melde uns Fehler und Verbesserungsvorschläge zur aktuellen Seite über dieses Formular. Vielen Dank ❤️
Footnotes
Credits Konformationen von Cyclohexan Grafik: Jawero, Ring-Flip-Mech, als gemeinfrei gekennzeichnet, Details auf Wikimedia Commons↩︎
Credits Energetische Betrachtung der Konformationen von Cyclohexan Grafik: Autor unbekannt.↩︎
Credits Instabile bicyclische Kohlenwasserstoffe, da Bredt’sche Regel verletzt Grafik: Jü, Brückenglieder S=5,6 V.1, CC0 1.0↩︎
