Alkohole
IMPP-Score: 3
Herstellung und Synthese von Alkoholen
Alkohole weisen eine breite Palette an wichtigen Eigenschaften auf, die sie in der Chemie zu wertvollen Substanzen machen. Ihre Herstellung erfolgt auf vielfältige Weise, jede mit ihren speziellen Reaktionsmechanismen und Anwendungsbereichen. Kommen wir nun zu einigen wichtigen Methoden der Alkoholsynthese.
Grignard-Reaktion und ihre Vielseitigkeit in der Alkoholsynthese
Eine wichtige Route zur Synthese von Alkoholen ist die Grignard-Reaktion, welche Magnesiumorganyle als Reagenzien verwendet. Diese Reaktion ermöglicht insbesondere die Herstellung von:
- Primären Alkoholen durch die Reaktion mit Formaldehyd.
- Sekundären Alkoholen beim Einsatz von Aldehyden, die nicht formaldehyde sind.
- Tertiären Alkoholen durch Umsetzung von Carbonsäureestern.
Die Grignard-Reaktion spielt beim IMPP eine bedeutende Rolle, und es ist wichtig, den Reaktionsmechanismus und die Art des gebildeten Alkohols zu verstehen.
Primäre Alkohole können effizient durch Reaktion von Grignard-Reagenzien mit Formaldehyd hergestellt werden. Das Produkt dieser Synthese ist häufig ein Thema in Prüfungsfragen.
Synthese von mehrwertigen Alkoholen
Beispiele für die Synthese mehrwertiger Alkohole umfassen:
- Glycerol (einen dreiwertigen Alkohol) wird aus den Vorstufen Glycerin oder mehrere Schritte umfassenden biotechnologischen Prozessen gewonnen.
- Zuckeralkohole wie Sorbit und Ribit werden durch Reduktion der korrespondierenden Zucker erhalten.
Wissenswert ist, dass Methanol aus der Destillation von Holz gewonnen werden kann, obwohl industriell hauptsächlich aus synthetischen Prozessen (z.B. aus Synthesegas) stammt.
Synthese von sekundären und tertiären Alkoholen
Sekundäre Alkohole lassen sich in der Regel aus Aldehyden oder Ketonen durch Reduktionsreaktionen herstellen - mittels Hydrierung oder durch Verwendung von Reduktionsmitteln wie Natriumborhydrid (NaBH4).
Tertiäre Alkohole können in der Regel nicht durch direkte Hydrierung einer Carbonsäure hergestellt werden, sondern entstehen oft durch komplexere Wege, wie die doppelte Grignard-Reaktion mit Estern. Diese oft prüfungsrelevante Tatsache sollte besonders beachtet werden.
Tertiäre Alkohole entstehen nicht durch einfache Hydrierung von Carbonsäuren. Ein gutes Verständnis für die spezifischen Synthesewege tertiärer Alkohole ist daher für das Examen essentiell.
Spezifische Synthesemethoden für die einzelnen Alkohol-Typen
Bei der Betrachtung der Synthese von Alkoholen sind folgende Methoden hervorzuheben:
- Nukleophile Substitution an Halogenalkanen: Vor allem über den SN2-Mechanismus, bei dem ein Halogenalkan mit einer Hydroxidionen-Quelle reagiert, wodurch ein Alkohol entsteht.
- Reduktion von Carbonylverbindungen: Ein primäres Kohlenstoffatom in Verbindung mit einer Carbonylgruppe (\(\text{C=O}\)) kann zu einem sekundären Alkohol reduziert werden.
- Oxidation von Alkenen: Durch Hydratisierungsreaktionen unter säurekatalysierten Bedingungen können aus Alkenen Alkohole gebildet werden.
Selektive Oxidation und ihre Anwendung
Ein weiterer wichtiger Punkt ist die selektive Oxidation, bei dem beispielsweise mit Pyridiniumchlorochromat (PCC) aus primären Alkoholen Aldehyde entstehen können, ohne dass diese weiter zu Carbonsäuren oxidiert werden.
Die Umsetzung von primären Alkoholen mit PCC führt zu Aldehyden. Dies ist ein Schlüsselprinzip für Reaktionen mit Alkoholen, das das IMPP gerne betont.
Alkoholate und ihre Bedeutung
Abschließend wollen wir die Erzeugung von Alkoholaten, beispielsweise Natriumethanolat, beleuchten. Diese reagieren stark basisch und nukleophil und spielen eine tragende Rolle in einer Vielzahl von Reaktionen, wie z.B. bei der Williamson-Ethersynthese oder als Zwischenprodukte bei der Entstehung von Enolaten.
Alkoholate können als Starter für wichtige Reaktionen im organischen Syntheselabor dienen – ein Verständnis ihrer Eigenschaften und Reaktionen ist zwingend notwendig.
Schlussendliche Bewertungen
Das Examen wird das Verständnis der Anwendung und Umsetzung der obigen Prinzipien prüfen. Daher ist es wesentlich, die Reaktionsmechanismen, den Kontext und die Ergebnisse dieser Reaktionen gründlich zu studieren. Achte also darauf, die vielfältigen Wege der Alkoholsynthese nicht nur zu kennen, sondern durchdringen zu können. Dies ist der Schlüssel, um im Examen erfolgreich zu sein.
Eigenschaften von Alkoholen
Alkohole sind definiert als organische Verbindungen, die eine oder mehrere Hydroxygruppen (-OH) enthalten. Diese Hydroxygruppen sind charakteristisch für die Eigenschaften der Alkohole und beeinflussen deren physische und chemische Verhaltensweisen maßgeblich. In diesem Abschnitt fokussieren wir uns ausschließlich auf die spezifischen Eigenschaften und die Nomenklatur von Alkoholen.
Wasserstoffbrückenbindungen und Siedepunkt
Die Hydroxygruppen von Alkoholen ermöglichen Wasserstoffbrückenbindungen, die eine starke intermolekulare Anziehungskraft darstellen. Dadurch haben Alkohole, im Vergleich zu hydrophoben organischen Verbindungen gleicher molarer Masse, deutlich höhere Siedepunkte. Zum Beispiel hat Ethanol einen Siedepunkt von etwa 78°C, während das vergleichbare Alkan Ethan nur bei etwa -89°C siedet. Diese Eigenschaft macht Alkohole unter anderem interessant für Anwendungen, bei denen Lösemittel mit höheren Siedepunkten benötigt werden.
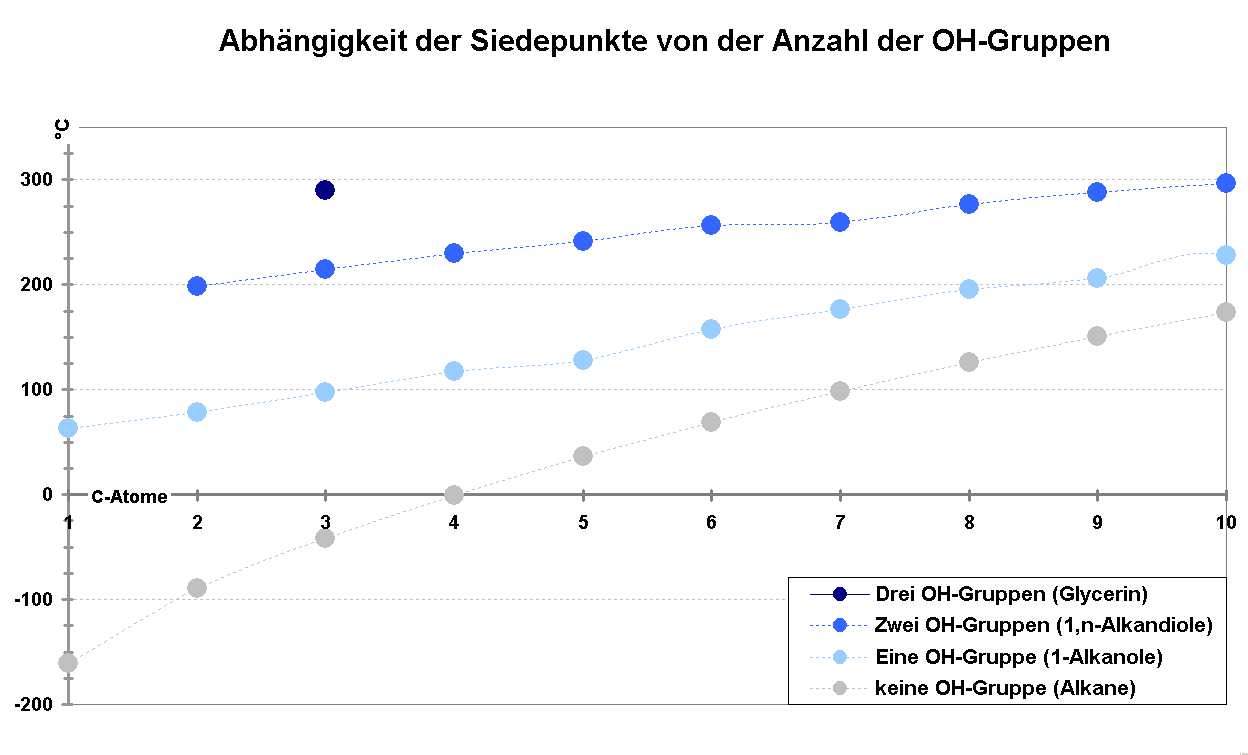
Das IMPP fragt gerne nach den Auswirkungen von Wasserstoffbrückenbindungen auf die Siedepunkte von Alkoholen. Verstehe daher gut, warum Alkohole höhere Siedepunkte als vergleichbare Alkane haben.
Löslichkeit in Wasser
Kleine Alkohole wie Methanol und Ethanol sind sehr gut wasserlöslich. Dies liegt zum einen an der Fähigkeit zur Ausbildung von Wasserstoffbrückenbindungen mit Wassermolekülen. Zum anderen reduziert die Polarität der Hydroxygruppe die Gesamtlipophilie des Moleküls. Mit steigender Kettenlänge der Alkylgruppe nimmt die Wasserlöslichkeit allerdings ab, da der hydrophobe Charakter der Kohlenwasserstoffkette stärker zur Geltung kommt.
Primäre, sekundäre und tertiäre Alkohole
Der Strukturtyp des Alkohols wird durch das Kohlenstoffatom bestimmt, an das die Hydroxygruppe gebunden ist:
- Primäre Alkohole haben eine Hydroxygruppe, die an ein Kohlenstoffatom gebunden ist, das nur ein weiteres Kohlenstoffatom trägt. Ein Beispiel hierfür wäre Ethanol (CH₃CH₂OH).
- Sekundäre Alkohole haben die Hydroxygruppe an einem Kohlenstoffatom, das an zwei andere Kohlenstoffatome gebunden ist, wie bei Isopropanol (CH₃CHOHCH₃).
- Tertiäre Alkohole besitzen eine Hydroxygruppe an einem Kohlenstoffatom, das mit drei anderen Kohlenstoffatomen verbunden ist, zum Beispiel 2-Methylpropan-2-ol ((CH₃)₃COH).
Das IMPP fragt häufig nach der Unterscheidung von primären, sekundären und tertiären Alkoholen. Sichere dir Punkte, indem du diese Strukturen erkennst!
Mehrwertige Alkohole - Diolen und Triole
Diolen und Triole enthalten zwei bzw. drei Hydroxygruppen. Sie spielen eine wichtige Rolle in der Polymerchemie und als Zwischenprodukte in biochemischen Prozessen. Glycerol, ein Triol, ist ein Grundbaustein für Fette und Öle. Diolen, wie Ethandiol (Ethylenglykol), finden Verwendung als Frostschutzmittel und bei der Herstellung von Polyestern.
Spezialfälle und bekannte Alkohole
Neben Struktur und Nomenklatur werden im IMPP auch spezifische Alkohole wie Methanol, Ethanol und Glycerol sowie Zuckeralkohole wie Sorbit besprochen. Methanol ist bekannt für seine Toxizität und wird in industriellen Prozessen verwendet, während Ethanol das Hauptprodukt der alkoholischen Gärung und ein gebräuchliches Desinfektionsmittel ist.
Vertraut euch mit den speziellen Eigenschaften und der Nutzung bekannter Alkohole wie Methanol und Ethanol. Diese Details sind beliebte Prüfungsinhalte.
Reaktionen von Alkoholen
Alkohole sind vielseitige Verbindungen in der organischen Chemie und können in verschiedenste Substanzklassen umgewandelt werden. Sie reagieren dabei aufgrund ihrer funktionellen Hydroxygruppe (\(-OH\)) oft über spezifische Mechanismen, die von der Stellung der Hydroxygruppe und der Art des Alkohols (primär, sekundär oder tertiär) abhängen.
Oxidation von Alkoholen
Die Oxidation von Alkoholen ist eine wichtige Reaktion, die es ermöglicht, aus Alkoholen Aldehyde, Ketone oder Carbonsäuren zu erzeugen.
- Primäre Alkohole oxidieren zuerst zu Aldehyden und können weiter zu Carbonsäuren oxidiert werden.
- Sekundäre Alkohole oxidieren zu Ketonen und bleiben dabei, da sie keine Wasserstoffatome am Kohlenstoff der Hydroxygruppe haben, die weiter oxidiert werden könnten.
- Tertiäre Alkohole lassen sich aufgrund der mangelnden Wasserstoffatome am oxidationsempfindlichen Kohlenstoff nicht durch einfache Oxidationsmittel oxidieren.
Es ist wichtig, dass du das IMPP oft nach der Oxidation von Ethanol zu fragen scheint, insbesondere im Zusammenhang mit der Umwandlung dieses Alltagsalkohols zu Chloroform.
Verstehe gut, wie primäre Alkohole weiter zu Aldehyden und Carbonsäuren oxidiert werden können, während sekundäre Alkohole bei Ketonen stoppen.
Spezialfälle: Oxidation und Reaktion von Methanol und Ethanol
- Methanol kann zu Formaldehyd und weiter zu Ameisensäure oxidiert werden.
- Ethanol kann zu Chloroform und weiteren Chemikalien umgesetzt werden.
Umwandlung in Alkylhalogenide
Alkohole können durch Reaktion mit Halogenwasserstoffsäuren wie HI oder Thionylchlorid (SOCl2) in Alkylhalogenide umgewandelt werden. Diese Reaktionen verlaufen oft über einen nukleophilen Substitutionsmechanismus (SN1 oder SN2).
Für das IMPP scheint die Umwandlung in Halogenide ein beliebtes Prüfungsthema zu sein, insbesondere die Reaktion von Alkoholen mit SOCl2.
Bildung von Ethern und Estern
- Ether können durch die Williamson-Ethersynthese gebildet werden, die eine nukleophile Substitution eines Halogenalkans mit einem Alkoholation umfasst.
- Ester entstehen durch Reaktion eines Alkohols mit einer Carbonsäure im Prozess der Veresterung.
Die Synthese von Ethern und Estern ist ein Kernelement der organischen Chemie. Das IMPP fragt oft nach diesen Transformationen, da sie Grundlagen für weitere organisch-chemische Reaktionen sind.
Dehydratisierung und Bildung von Enolaten
- Dehydratisierung: Alkohole können durch Erwärmung mit einem geeigneten Katalysator wie Schwefelsäure Wasser abspalten, um Alkene zu bilden. Der Mechanismus kann entweder ein E1 (häufig bei tertiären Alkoholen) oder ein E2 (häufig bei sekundären und primären Alkoholen) sein.
- Bildung von Enolaten: Alkoholate (Alkohol + starke Base wie Natriumhydrid) können Enolate bilden, die sehr reaktive Spezies in der organischen Synthese sind.
Verwendung von Alkoholen als Schutzgruppe
Alkohole können als Schutzgruppe in der organischen Synthese dienen, indem sie funktionelle Gruppen wie Carbonylverbindungen vor unerwünschten Reaktionen schützen.
Es ist enorm wichtig, Strategien für das Schützen und Entschützen von funktionellen Gruppen zu kennen, denn das IMPP prüft häufig das Wissen um selektive Umsetzungen in der Synthese.
Zusammenfassung
Feedback
Melde uns Fehler und Verbesserungsvorschläge zur aktuellen Seite über dieses Formular. Vielen Dank ❤️
Footnotes
Credits Allgemeine Struktur der Alkohole Grafik: NEUROtiker, Alkohol - Alcohol, als gemeinfrei gekennzeichnet, Details auf Wikimedia Commons↩︎
Credits Grignard-Reaktionsmechanismus Grafik: Дёрте Вилкен, Grignard Reaktion Übersicht2, als gemeinfrei gekennzeichnet, Details auf Wikimedia Commons↩︎
Credits Abhängigkeit der Siedepunkte von der Anzahl der OH-Gruppen Grafik: Peter Krimbacher, Diagramm-Abhängigkeit des Sdp von Anzahl OH-Gruppen, CC BY-SA 2.0 DE↩︎
